Court of Appeal 28 mei 2015, IEF 14972; [2015] EWCA Civ 556 (Warner-Lambert tegen Actavis)
 Met samenvatting van Rutger Kleemans, Freshfields Bruckhaus Deringer LLP. Engeland. De Court of Appeal in London (Floyd LJ) heeft een beslissing gegeven in de zaak tussen Warner-Lambert en Actavis (pregabaline). Deze beslissing is van belang omdat – alhoewel het geen bodemzaak is maar het een door Warner Lambert ingesteld hoger beroep betreft tegen een in eerste instantie geweigerde voorlopige voorziening – de Engelse rechter in detail ingaat op (i) het gebruik van zogenaamde skinny labels, (ii) directe en indirecte inbreuk met skinny labels op tweede medische indicatie octrooien, (iii) de constructie en uitleg van Swiss-type conclusies en (iv) de feitelijke problematiek die zich voordoet bij het voorschrijven en vergoeden van geneesmiddelen met een skinny label.
Met samenvatting van Rutger Kleemans, Freshfields Bruckhaus Deringer LLP. Engeland. De Court of Appeal in London (Floyd LJ) heeft een beslissing gegeven in de zaak tussen Warner-Lambert en Actavis (pregabaline). Deze beslissing is van belang omdat – alhoewel het geen bodemzaak is maar het een door Warner Lambert ingesteld hoger beroep betreft tegen een in eerste instantie geweigerde voorlopige voorziening – de Engelse rechter in detail ingaat op (i) het gebruik van zogenaamde skinny labels, (ii) directe en indirecte inbreuk met skinny labels op tweede medische indicatie octrooien, (iii) de constructie en uitleg van Swiss-type conclusies en (iv) de feitelijke problematiek die zich voordoet bij het voorschrijven en vergoeden van geneesmiddelen met een skinny label.
De Court of Appeal kan zich niet verenigen met de eerdere beslissingen van Arnold J ([2015] EWHC 72 (Pat) van 21 januari 2015, [2015] EWCH] 223 (Pat) en [2015] EWCH 249 (Pat) van 6 februari 2015) zowel waar het betreft Arnolds motivatie met betrekking tot directe als indirecte inbreuk. Ten aanzien van indirecte inbreuk is interessant dat Floyd drie redenen geeft om de beslissing van Arnold (voorlopig) te herzien en hij verwijst naar lopende procedures betreffende hetzelfde onderwerp in Europa waaronder Nederland (voor de goede orde; ik treed zelf op in de procedure van Novartis tegen Sun waarnaar verwezen wordt – RK):
Indirect infringement
134 It will be seen that courts of two member states have, at least in provisional proceedings, granted relief to prevent what they considered to be indirect infringement of Swiss claims without any express indication of how they considered that the invention would be put into effect.
135 I agree that there are difficulties with the indirect infringement claim for the reason which the judge gave, namely the absence of a downstream event which, as a whole, can be regarded as putting the invention into effect. However, for three reasons, each of which is in my judgment sufficient, I would allow the indirect infringement case to go to trial.
136 The first reason is that which I have already given, namely that the courts of two EPC member states considering this same question have held that, at face value, indirect infringement can arise in these circumstances.
137 The second reason is that, if, as I have held, there is a case of threatened or actual infringement of the process claim under section 60(1)(b), then it follows that dealings downstream in the direct product of the process are also infringements under section 60(1)(c). Although this may not add anything to the direct infringement case, it is wrong to strike it out as a viable additional cause of action.
138 The third reason is that I consider it is arguable to say that when section 60(2) speaks of “putting the invention into effect”, it may be legitimate to look not just at whether any one person is carrying out the invention in a sense which would give rise to liability of that person for an act of infringement. It may be that the invention is put into effect if pregabalin is manufactured by one person and supplied to another who intentionally uses it for the treatment of pain. In those circumstances, a person who supplies pregabalin with the requisite knowledge (i.e. that prescribed in section 60(2) itself) does provide means suitable and intended to put the invention into effect, albeit by the combination of manufacturer and user, rather than by any one person alone. It may be that this is the reasoning which underlies the decisions in the Dutch and German cases which I have referred to.
139 An analogous problem arises where one step of a two step process is carried out by A and the second step is carried out by B. Absent a claim of joint tortfeasance, could it not be said that by supplying the result of the first step to B, A is contributing to putting the invention into effect (by A and B together)?
140 It follows that I would allow the appeal against the striking out of the section 60(2) claim.
Niettemin wordt het door Werner Lambert gevorderde voorlopige verbod geweigerd. De belangrijkste reden hiervoor is dat de NHS (National Health Service) in een separate door Warner Lambert ingestelde procedure [2015] EWCH 485 (Pat)] was veroordeeld tot het uitvaardigen van richtlijnen aan voorschrijvers op grond waarvan aannemelijk is dat gebruik van generiek pregabaline voor de geoctrooieerde indicaties voorkomen kan worden en geen inbreuk (meer) plaatsvindt.
Rutger Kleemans



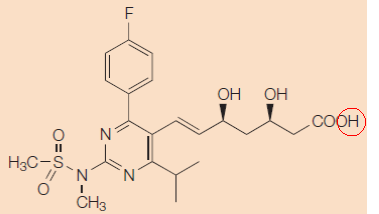 Octrooirecht. ABC. Directe octrooiinbreuk. Uitleg octrooiconclusie en toegevoegde materie. Het ABC, gebaseerd op
Octrooirecht. ABC. Directe octrooiinbreuk. Uitleg octrooiconclusie en toegevoegde materie. Het ABC, gebaseerd op  Octrooirecht. Farmaceutisch octrooi; Bereidingswijze van drospirenon (werkzame stof in een anticonceptiepil). Zie eerder
Octrooirecht. Farmaceutisch octrooi; Bereidingswijze van drospirenon (werkzame stof in een anticonceptiepil). Zie eerder  Uitspraak ingezonden door Marleen van den Horst, David Mulder,
Uitspraak ingezonden door Marleen van den Horst, David Mulder,  Octrooi. Geen (directe) inbreuk. Onrechtmatig handelen. Niet noodzakelijk. Carve out. WLC is houdster van het Europees octrooi
Octrooi. Geen (directe) inbreuk. Onrechtmatig handelen. Niet noodzakelijk. Carve out. WLC is houdster van het Europees octrooi 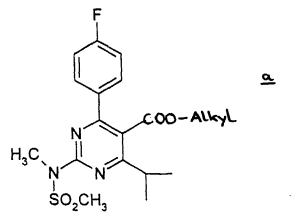 Octrooirecht. ABC. Afstandsleer. Shionogi is farmaceutische onderneming en houdster van ABC 300125 voor 'Rosuvastatinum, desgewenst in de vorm van een niet-toxisch farmaceutisch aanvaardbaar zout, in het bijzonder het calciumzout', voorheen houdster van EP471 'Pyrimidinederivaten als HMG-CoA-reductase-inhibitoren’. Resolution vordert met succes de partiële nietigheid van het octrooi en ABC vanwege toegevoegde materie; voor zover de bescherming ervan zich uitstrekt over andere producten dan in EP 471 genoemde niet-toxische farmaceutisch aanvaardbare zouten van rosuvastatine.
Octrooirecht. ABC. Afstandsleer. Shionogi is farmaceutische onderneming en houdster van ABC 300125 voor 'Rosuvastatinum, desgewenst in de vorm van een niet-toxisch farmaceutisch aanvaardbaar zout, in het bijzonder het calciumzout', voorheen houdster van EP471 'Pyrimidinederivaten als HMG-CoA-reductase-inhibitoren’. Resolution vordert met succes de partiële nietigheid van het octrooi en ABC vanwege toegevoegde materie; voor zover de bescherming ervan zich uitstrekt over andere producten dan in EP 471 genoemde niet-toxische farmaceutisch aanvaardbare zouten van rosuvastatine. Uitspraak ingezonden door namens Otto Swens en Ricardo Dijkstra,
Uitspraak ingezonden door namens Otto Swens en Ricardo Dijkstra,  Met samenvatting van Rutger Kleemans,
Met samenvatting van Rutger Kleemans, 













